- SELAMAT DATANG di Official Site SMA Negeri 1 Taman Sidoarjo Jawa Timur
Pengaruh Luas Permukaan Terhadap Laju Reaksi
Oleh : Dewi Nurmalasari
Selain suhu dan konsentrasi, luas permukaan zat padat juga berpengaruh besar terhadap laju reaksi kimia. Pengaruh ini terutama berlaku pada reaksi yang melibatkan zat padat dan zat cair atau gas, di mana reaksi terjadi di permukaan kontak antara kedua zat tersebut. Semakin luas permukaan zat padat yang bersentuhan dengan zat lain, semakin banyak partikel zat padat yang tersedia untuk bereaksi. Akibatnya, frekuensi tumbukan antarpartikel meningkat, sehingga reaksi berlangsung lebih cepat.
Menurut teori tumbukan, reaksi kimia terjadi ketika partikel-partikel pereaksi saling bertumbukan dengan energi yang cukup besar (energi aktivasi) dan dengan arah yang sesuai. Dalam zat padat, tumbukan hanya dapat terjadi di permukaan tempat partikel-partikel zat padat tersebut bersentuhan langsung dengan zat lain. Oleh karena itu, jika zat padat berbentuk bongkahan besar, hanya sebagian kecil partikel di permukaannya yang dapat ikut bereaksi, sementara partikel-partikel di bagian dalam belum terlibat. Namun, jika zat padat tersebut dipecah menjadi potongan-potongan kecil atau digiling menjadi serbuk, maka jumlah partikel yang berada di permukaan akan meningkat tajam, sehingga lebih banyak partikel yang dapat bertumbukan dengan pereaksi lainnya. Inilah sebabnya mengapa semakin luas permukaan suatu zat padat, laju reaksinya semakin cepat

Fenomena ini dapat dengan mudah diamati melalui berbagai contoh eksperimen sederhana di laboratorium. Salah satunya adalah reaksi antara magnesium (Mg) dengan asam klorida (HCl). Ketika pita magnesium utuh direaksikan dengan HCl, gelembung gas hidrogen (H₂) terbentuk secara perlahan. Namun, apabila magnesium tersebut dipotong kecil-kecil atau digosok hingga menjadi serbuk, gelembung gas akan terbentuk jauh lebih cepat. Hal ini terjadi karena pada serbuk magnesium, luas permukaan kontak antara logam dan larutan HCl menjadi lebih besar, sehingga tumbukan antara ion H⁺ dan atom magnesium lebih sering terjadi.
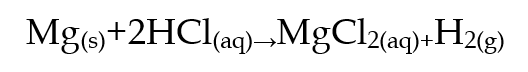
Contoh lainnya dapat dilihat pada reaksi pembakaran. Serbuk logam magnesium atau serbuk kayu terbakar jauh lebih cepat dibandingkan batang magnesium atau potongan kayu yang utuh. Hal ini disebabkan oleh luas permukaan serbuk yang jauh lebih besar, sehingga partikel-partikel zat mudah bereaksi dengan oksigen di udara. Prinsip yang sama juga digunakan dalam industri bahan bakar, di mana bahan bakar cair disemprotkan dalam bentuk kabut halus agar terbakar lebih cepat dan efisien.
Dengan demikian, dapat disimpulkan bahwa luas permukaan zat padat sangat memengaruhi laju reaksi kimia. Semakin luas permukaan kontak antara zat-zat pereaksi, semakin banyak partikel yang dapat saling bertumbukan, dan semakin cepat reaksi berlangsung. Prinsip ini tidak hanya penting dalam memahami konsep dasar kinetika kimia, tetapi juga sangat relevan dalam penerapan teknologi industri, proses pembakaran, serta berbagai fenomena alam dan kegiatan sehari-hari. (dewi)
https://nurmalasaridewi-72.medium.com/pengaruh-luas-permukaan-terhadap-laju-reaksi-58ef6775a6d7
Sumber Pustaka:
Munaspriyanto, 2022. KIMIA SMA/MA XI. Jakarta: Kementrian Pendidikan Kebudayaan Riset dan Teknologi
Moenandar Ismunaryo, 2018. Teori Kimia Dasar 1. Jakarta: Bina Prestasi Insani
Pertucci Ralph H, 1999. Kimia Dasar Prinsip dan Terapan Modern Edisi 4. Jakarta: Penerbit Erlangga





Komentar Terbaru