Dalam reaksi kimia, kecepatan terjadinya perubahan dari zat pereaksi menjadi produk disebut laju reaksi. Salah satu faktor penting yang memengaruhi laju reaksi adalah konsentrasi zat pereaksi. Konsentrasi menunjukkan jumlah partikel zat dalam suatu volume larutan. Semakin tinggi konsentrasi suatu zat, semakin banyak partikel yang terdapat dalam satuan volume, sehingga kemungkinan partikel-partikel tersebut saling bertumbukan menjadi lebih besar.
Menurut teori tumbukan, agar suatu reaksi kimia dapat berlangsung, partikel-partikel pereaksi harus bertumbukan dengan energi yang cukup besar (disebut energi aktivasi) dan dengan orientasi yang tepat. Tumbukan semacam ini disebut tumbukan efektif karena menghasilkan reaksi dan membentuk produk baru. Oleh karena itu, semakin sering terjadi tumbukan efektif, semakin cepat pula reaksi berlangsung.
Ketika konsentrasi pereaksi dinaikkan, jumlah partikel per satuan volume juga meningkat. Hal ini membuat jarak antarpartikel menjadi lebih dekat, sehingga dalam waktu yang sama, frekuensi tumbukan antara partikel-partikel pereaksi menjadi lebih sering. Akibatnya, jumlah tumbukan efektif bertambah, dan laju reaksi meningkat. Sebaliknya, jika konsentrasi pereaksi diturunkan, jumlah partikel dalam volume yang sama menjadi lebih sedikit, jarak antarpartikel lebih jauh, frekuensi tumbukan menurun, dan laju reaksi menjadi lebih lambat.

Fenomena ini dapat diamati melalui berbagai percobaan sederhana di laboratorium. Misalnya, pada reaksi antara magnesium (Mg) dan asam klorida (HCl), gas hidrogen (H₂) dihasilkan lebih cepat ketika larutan HCl yang digunakan lebih pekat. Pada HCl berkonsentrasi 4 M, gelembung gas hidrogen muncul lebih cepat dan banyak dibandingkan ketika menggunakan HCl 1 M. Hal ini menunjukkan bahwa peningkatan konsentrasi larutan mempercepat reaksi karena partikel asam yang bereaksi dengan logam magnesium jumlahnya lebih banyak.
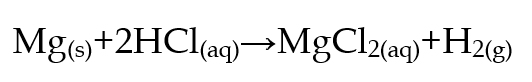
Contoh lain yang sering digunakan dalam pembelajaran adalah reaksi antara natrium tiosulfat (Na₂S₂O₃) dengan asam klorida (HCl). Pada percobaan ini, waktu yang dibutuhkan hingga larutan menjadi keruh (karena terbentuk endapan sulfur) digunakan untuk mengukur laju reaksi. Hasil pengamatan menunjukkan bahwa semakin tinggi konsentrasi HCl, semakin cepat larutan menjadi keruh, yang berarti reaksi berlangsung lebih cepat.
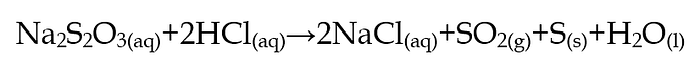
Hubungan antara konsentrasi dan laju reaksi ini dapat dijelaskan secara matematis melalui hukum laju reaksi. Jika laju reaksi dinyatakan dengan persamaan
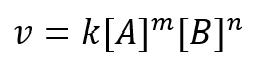
Keterangan:
v = laju reaksi (mol·L⁻¹·s⁻¹)
k = konstanta laju
m dan n = orde reaksi terhadap A dan B
Maka nilai orde reaksi (m dan n) menunjukkan sejauh mana konsentrasi reaktan memengaruhi laju reaksi. Bila suatu reaksi berorde satu terhadap zat A, maka peningkatan konsentrasi A dua kali lipat akan meningkatkan laju reaksi dua kali lipat. Jika berorde dua, peningkatan dua kali lipat konsentrasi akan mempercepat reaksi empat kali lipat.
Jika orde reaksi terhadap suatu zat = 1, maka peningkatan konsentrasi 2 kali akan melipatgandakan laju reaksi. Jika orde reaksi = 2, peningkatan konsentrasi 2 kali akan meningkatkan laju 4 kali lipat.
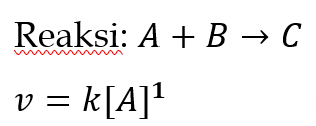
Contoh:
Jika konsentrasi [A] naik dari 0,1 M → 0,2 M, maka:
Laju reaksi menjadi dua kali lebih cepat.
Dalam kehidupan sehari-hari, pengaruh konsentrasi terhadap laju reaksi dapat ditemukan pada berbagai peristiwa. Misalnya, larutan pembersih yang lebih pekat bekerja lebih cepat melarutkan kotoran atau kerak logam. Dalam proses fermentasi makanan, kadar gula yang tinggi mempercepat reaksi yang melibatkan mikroorganisme hingga batas tertentu. Sebaliknya, pada proses pengawetan makanan, kadar air atau konsentrasi zat yang bereaksi dengan oksigen sengaja dikurangi agar laju reaksi pembusukan menjadi lebih lambat.
Dengan demikian, dapat disimpulkan bahwa konsentrasi merupakan salah satu faktor utama yang menentukan cepat atau lambatnya suatu reaksi kimia berlangsung. Melalui peningkatan konsentrasi, frekuensi tumbukan antarpartikel bertambah, jumlah tumbukan efektif meningkat, dan laju reaksi pun menjadi lebih besar.
https://nurmalasaridewi-72.medium.com/pengaruh-konsentrasi-terhadap-laju-reaksi-b347f90334a1
Sumber Pustaka:
Munaspriyanto, 2022. KIMIA SMA/MA XI. Jakarta: Kementrian Pendidikan Kebudayaan Riset dan Teknologi
Moenandar Ismunaryo, 2018. Teori Kimia Dasar 1. Jakarta: Bina Prestasi Insani
Pertucci Ralph H, 1999. Kimia Dasar Prinsip dan Terapan Modern Edisi 4. Jakarta: Penerbit Erlangga





Komentar Terbaru