Suhu merupakan salah satu faktor yang sangat berpengaruh terhadap kecepatan reaksi kimia. Pada dasarnya, reaksi kimia terjadi karena adanya tumbukan antarpartikel pereaksi. Namun, tidak semua tumbukan menghasilkan reaksi. Agar reaksi dapat terjadi, tumbukan antarpartikel harus memiliki energi minimum tertentu yang disebut energi aktivasi (Ea). Energi aktivasi inilah yang diperlukan untuk memutuskan ikatan lama dan membentuk ikatan baru.
Ketika suhu suatu sistem dinaikkan, energi kinetik rata-rata partikel meningkat. Partikel bergerak lebih cepat, frekuensi tumbukan meningkat, dan yang terpenting — semakin banyak partikel yang memiliki energi sama atau lebih besar dari energi aktivasi. Akibatnya, jumlah tumbukan efektif meningkat, dan laju reaksi menjadi lebih cepat. Sebaliknya, ketika suhu diturunkan, energi kinetik partikel berkurang. Gerakan partikel menjadi lebih lambat, frekuensi tumbukan menurun, dan hanya sedikit partikel yang memiliki energi cukup untuk melewati energi aktivasi. Akibatnya, reaksi menjadi lebih lambat.

Menurut teori tumbukan:
a. Partikel bereaksi hanya jika mereka bertumbukan dengan energi ≥ energi aktivasi.
b. Peningkatan suhu tidak hanya meningkatkan jumlah tumbukan, tetapi juga meningkatkan proporsi partikel yang memiliki energi lebih tinggi dari Ea.
Fenomena ini dapat dijelaskan menggunakan kurva distribusi energi Maxwell-Boltzmann, yang menunjukkan jumlah partikel pada berbagai tingkat energi.
· Pada suhu rendah, kurva sempit dan puncaknya tinggi hanya sedikit partikel yang melewati energi aktivasi.
· Ketika suhu meningkat, kurva melebar dan bergeser ke kanan lebih banyak partikel melewati energi aktivasi, sehingga reaksi berlangsung lebih cepat.
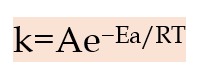
Hubungan antara suhu dan laju reaksi secara kuantitatif dijelaskan oleh persamaan Arrhenius:
(k) = konstanta laju reaksi
(A) = faktor frekuensi tumbukan
(Ea) = energi aktivasi (J/mol)
(R) = konstanta gas (8,314 J/mol·K)
(T) = suhu mutlak (Kelvin)
Persamaan ini menunjukkan bahwa kenaikan suhu (T) akan menaikkan nilai k, karena nilai eksponen menjadi kurang negatif. Artinya, konstanta laju meningkat eksponensial terhadap kenaikan suhu, bukan hanya linier.
Secara empiris, kenaikan suhu sebesar 10°C umumnya dapat melipatgandakan atau melipattigakan laju reaksi — walau nilai ini bervariasi tergantung jenis reaksi dan energi aktivasinya.
a. Reaksi Natrium Tiosulfat dan Asam Klorida

Reaksi antara larutan natrium tiosulfat (Na₂S₂O₃) dengan HCl menghasilkan endapan sulfur:
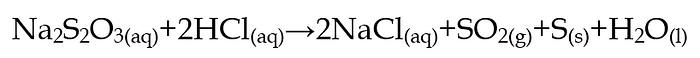
Ketika suhu larutan dinaikkan (misalnya dari 25°C ke 40°C), larutan menjadi keruh lebih cepat. Hal ini karena partikel tiosulfat dan ion H⁺ bergerak lebih cepat dan lebih sering bertumbukan dengan energi cukup untuk menghasilkan sulfur padat.
b. Reaksi Enzimatis dan Pembusukan
Dalam proses biokimia, seperti fermentasi atau pembusukan, suhu yang lebih tinggi mempercepat reaksi karena aktivitas enzim meningkat. Namun, jika suhu terlalu tinggi, enzim dapat terdenaturasi dan reaksi justru berhenti. Oleh karena itu, suhu optimum menjadi penting dalam industri makanan, seperti proses pembuatan roti atau yogurt.
c. Kehidupan Sehari-hari
Makanan cepat basi di tempat panas karena reaksi kimia pembusukan berlangsung lebih cepat.
Di industri, reaksi kimia seperti pembuatan amonia (proses Haber) dilakukan pada suhu tinggi untuk mempercepat pembentukan produk, namun dikontrol agar tidak menghambat kesetimbangan.
Pada suhu tinggi, lebih banyak partikel memiliki energi di atas garis tersebut, sehingga jumlah partikel yang “melompati” penghalang meningkat inilah yang mempercepat laju reaksi. Dalam konteks pembelajaran dan kehidupan nyata, pemahaman tentang pengaruh suhu terhadap laju reaksi membantu murid memahami mengapa kontrol suhu penting dalam industri kimia, farmasi, dan pangan. Misalnya:
· Di industri pupuk, suhu tinggi digunakan untuk mempercepat pembentukan amonia dari gas nitrogen dan hidrogen.
· Di rumah tangga, penyimpanan makanan dalam lemari pendingin bertujuan memperlambat reaksi kimia pembusukan, sehingga makanan lebih tahan lama.
Peningkatan suhu menyebabkan partikel-partikel pereaksi bergerak lebih cepat dan memiliki energi kinetik lebih besar. Akibatnya, frekuensi tumbukan meningkat dan lebih banyak partikel memiliki energi ≥ energi aktivasi, sehingga reaksi berlangsung lebih cepat. Sebaliknya, penurunan suhu mengurangi energi kinetik dan jumlah tumbukan efektif, menyebabkan reaksi berjalan lebih lambat. Dengan demikian, suhu berperan penting sebagai pengendali laju reaksi, baik dalam proses alami maupun dalam penerapan teknologi dan industri. (dewi)
https://nurmalasaridewi-72.medium.com/pengaruh-suhu-terhadap-laju-reaksi-06582665ebbe
Sumber Pustaka:
Munaspriyanto, 2022. KIMIA SMA/MA XI. Jakarta: Kementrian Pendidikan Kebudayaan Riset dan Teknologi
Moenandar Ismunaryo, 2018. Teori Kimia Dasar 1. Jakarta: Bina Prestasi Insani
Pertucci Ralph H, 1999. Kimia Dasar Prinsip dan Terapan Modern Edisi 4. Jakarta: Penerbit Erlangga





Komentar Terbaru