Dalam banyak reaksi kimia, kecepatan reaksi tidak hanya dipengaruhi oleh suhu, konsentrasi, dan luas permukaan, tetapi juga oleh adanya katalis. Katalis adalah suatu zat yang mempercepat laju reaksi kimia tanpa ikut habis bereaksi. Artinya, katalis berperan dalam proses reaksi tetapi pada akhir reaksi jumlah dan sifatnya tetap. Walaupun katalis tidak mengubah hasil akhir reaksi atau keseimbangan kimia, zat ini sangat penting karena dapat menurunkan energi aktivasi (Ea), yaitu energi minimum yang dibutuhkan agar tumbukan antarpartikel menghasilkan reaksi.
Menurut teori tumbukan dan konsep energi aktivasi, reaksi kimia terjadi ketika partikel-partikel pereaksi bertumbukan dengan energi yang cukup untuk memutuskan ikatan lama dan membentuk ikatan baru. Namun, tidak semua tumbukan memiliki energi yang cukup tinggi untuk melampaui penghalang energi aktivasi ini. Katalis bekerja dengan menyediakan jalur reaksi alternatif yang memiliki energi aktivasi lebih rendah, sehingga lebih banyak partikel pereaksi yang memiliki energi cukup untuk bereaksi pada suhu yang sama. Akibatnya, frekuensi tumbukan efektif meningkat dan laju reaksi menjadi lebih cepat.
Perbedaan ini dapat digambarkan dalam diagram energi potensial. Pada reaksi tanpa katalis, puncak energi aktivasi lebih tinggi, sedangkan pada reaksi dengan katalis, puncak energi menjadi lebih rendah. Kedua jalur reaksi tersebut menghasilkan energi total (ΔH) yang sama, namun waktu yang diperlukan untuk mencapai produk berbeda karena jalur dengan katalis berlangsung lebih cepat.
Contoh Reaksi dengan Katalis
a. Penguraian Hidrogen Peroksida (H₂O₂)
Hidrogen peroksida secara alami terurai menjadi air dan oksigen:
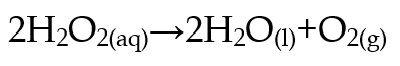
Reaksi ini berlangsung sangat lambat pada suhu kamar. Namun, dengan menambahkan katalis MnO₂ (mangan dioksida), reaksi terjadi jauh lebih cepat, ditandai dengan munculnya gelembung gas oksigen. Dalam reaksi ini, MnO₂ tidak ikut bereaksi dan dapat digunakan kembali setelah proses selesai.

b. Reaksi Pembentukan Amonia (Proses Haber)
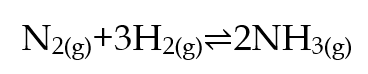
Reaksi antara gas nitrogen dan hidrogen berlangsung sangat lambat meskipun pada suhu tinggi. Dalam industri, digunakan katalis besi (Fe) untuk mempercepat pembentukan amonia tanpa mengubah posisi kesetimbangan. Kehadiran katalis memungkinkan proses berlangsung pada suhu dan tekanan yang lebih rendah, sehingga menghemat energi dan biaya produksi.
c. Reaksi di Dalam Tubuh Makhluk Hidup (Enzim Sebagai Katalis Biologis)
Di dalam tubuh, hampir semua reaksi biokimia dikatalisis oleh enzim. Misalnya, enzim catalase dalam hati dan darah mempercepat penguraian H₂O₂ yang bersifat racun menjadi air dan oksigen. Tanpa bantuan enzim, reaksi tersebut akan berlangsung terlalu lambat untuk mendukung kehidupan.
Jenis-Jenis Katalis
a. Katalis Homogen
b. Katalis Heterogen
Katalis berada pada fase berbeda dengan pereaksi. Contoh: Besi (Fe) padat pada reaksi gas N₂ dan H₂ dalam proses Haber.
c. Katalis Biologis (Enzim)
Katalis alami yang bekerja sangat spesifik pada reaksi tertentu dalam makhluk hidup.
Aplikasi Katalis dalam Kehidupan dan Industri
Peran katalis sangat luas dan vital, baik dalam proses industri maupun dalam sistem biologis, di antaranya:
a. Industri Otomotif: Katalis logam mulia seperti platinum (Pt) dan paladium (Pd) digunakan dalam catalytic converter kendaraan bermotor untuk mengubah gas beracun seperti CO dan NO menjadi gas yang tidak berbahaya (CO₂ dan N₂).
b. Industri Pupuk: Besi sebagai katalis mempercepat produksi amonia, bahan dasar pupuk urea.
c. Industri Pangan: Nikel (Ni) digunakan dalam proses hidrogenasi minyak nabati menjadi margarin.
d. Sistem Biologis: Enzim-enzim seperti amilase, lipase, dan protease mempercepat reaksi pencernaan makanan tanpa ikut habis.
Adanya katalis, reaksi yang semula lambat dan tidak efisien dapat berlangsung lebih cepat, hemat energi, dan ramah lingkungan.
Katalis dapat diibaratkan seperti jembatan yang mempermudah perjalanan. Tanpa jembatan, seseorang harus menempuh jalan panjang dan melelahkan (energi aktivasi tinggi). Dengan adanya jembatan (katalis), perjalanan menjadi lebih singkat dan mudah (energi aktivasi rendah). Namun, jembatan itu sendiri tidak berubah dan tetap dapat digunakan oleh orang lain setelahnya.
Katalis merupakan zat yang mempercepat laju reaksi kimia dengan cara menurunkan energi aktivasi dan menyediakan jalur reaksi alternatif yang lebih mudah dilalui partikel pereaksi. Meskipun katalis ikut terlibat dalam proses reaksi, zat ini tidak mengalami perubahan kimia permanen. Keberadaan katalis sangat penting, baik dalam reaksi-reaksi industri, proses lingkungan, maupun di dalam tubuh makhluk hidup. Tanpa katalis, banyak proses kimia penting akan berlangsung terlalu lambat untuk dimanfaatkan secara praktis. (dewi)
https://nurmalasaridewi-72.medium.com/pengaruh-katalis-terhadap-laju-reaksi-0a950cd8b198
Sumber Pustaka:
Munaspriyanto, 2022. KIMIA SMA/MA XI. Jakarta: Kementrian Pendidikan Kebudayaan Riset dan Teknologi
Moenandar Ismunaryo, 2018. Teori Kimia Dasar 1. Jakarta: Bina Prestasi Insani
Pertucci Ralph H, 1999. Kimia Dasar Prinsip dan Terapan Modern Edisi 4. Jakarta: Penerbit Erlangga





Komentar Terbaru